
目的:
为了规范我院临床试验文档管理,确保文档的完整性、可追溯性和合规性。
适用范围:
适用于在我院开展的注册类临床试验项目需受控文件,如:疗效评估量表、生物样本相关表格、生命体征记录表等。
具体流程:
一、 账号管理
1. 临床研究电子文档管理系统(以下简称“文档管理系统”)由系统管理员统一负责账号的注册审核与权限管理。
2. 用户可通过文档管理系统(访问网址:https://etmf-xy3.seedata.com.cn/sign-in)注册或登录账号。
3.注册账后请将以下信息发送给对应科室的质控员(你的姓名,联系方式;项目的申办方名称,公司联系人及联系方式;CRO名称,公司联系人及联系方式(需注明是申办方还是CRO)),质控员会将您的信息发给信息管理员进行审核,审核通过后您可以登录。
二、 项目管理
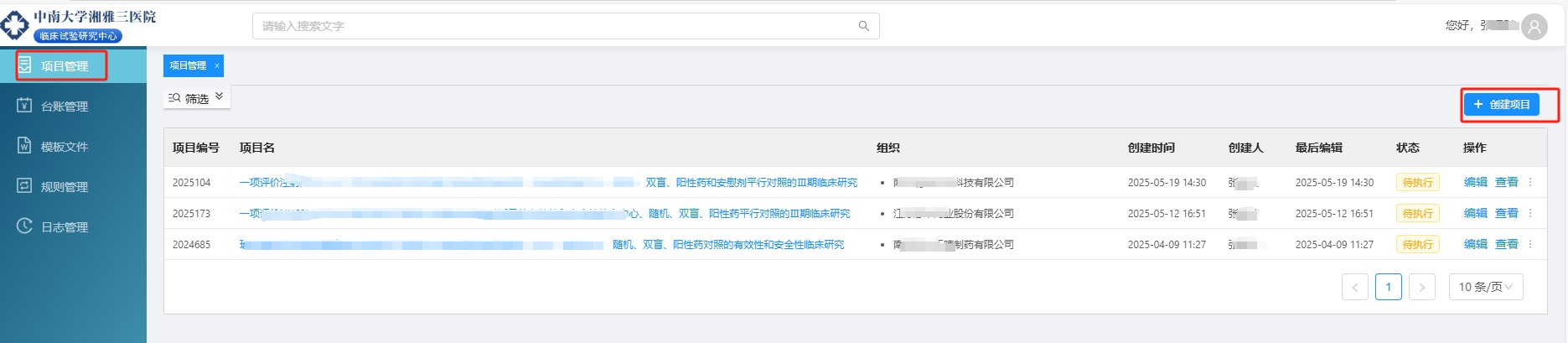
1. 研究团队成员在文档管理系统的【项目管理】模块点击菜单【创建项目】,选择【申办方】,填写【项目名】(项目全称)、【项目编号】(CTRI系统中的流水号)、【方案编号】等必要信息。如创建后发现填写的信息有误,可通过此页面的【编辑】操作更新。
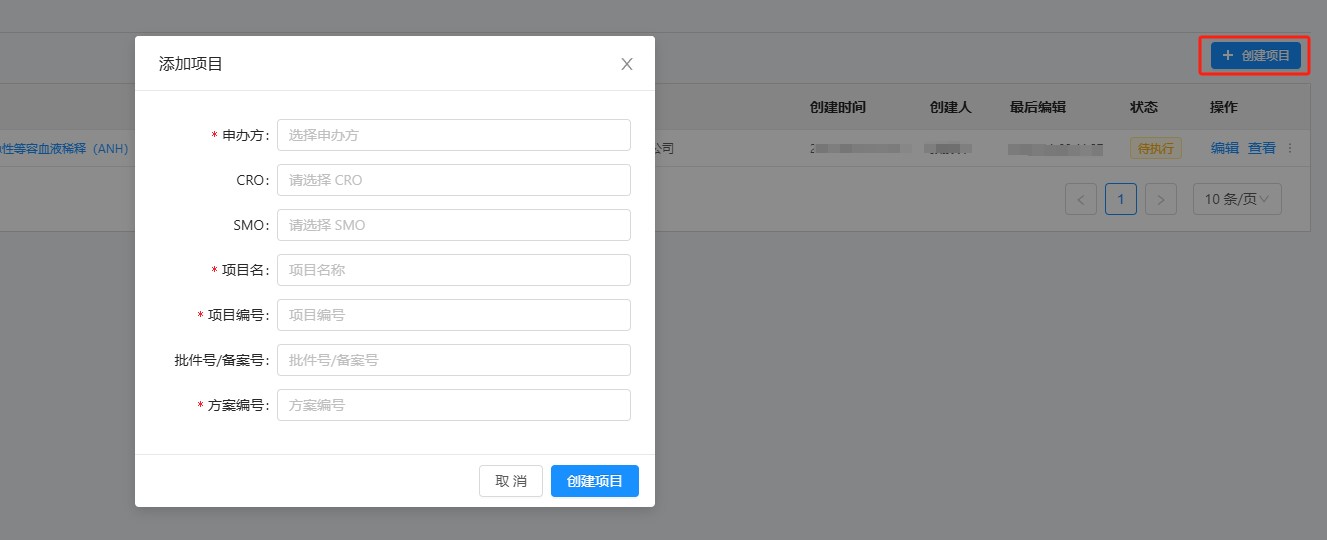
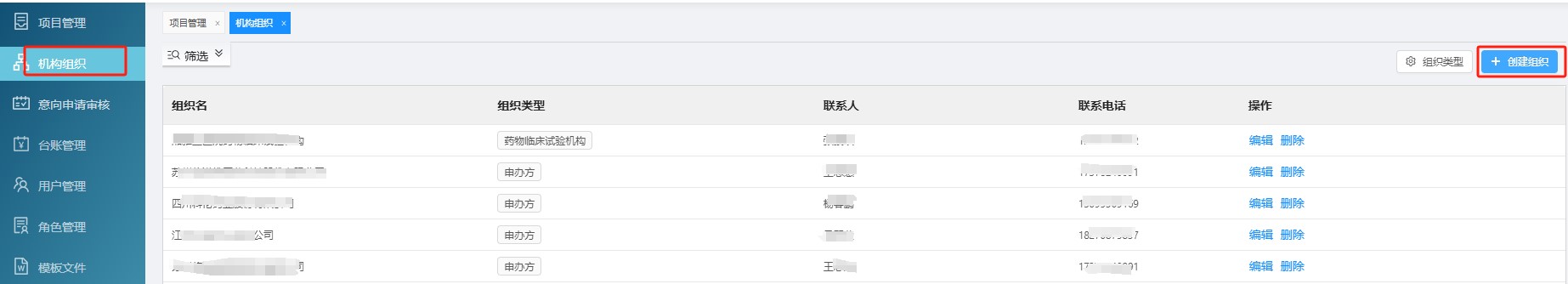
2. 若申办方、CRO、SMO公司未在系统备案(即在创建项目时无法选择到相应公司),需联系系统管理员通过文档管理系统的【机构组织】模块完成公司备案后,方可创建项目。
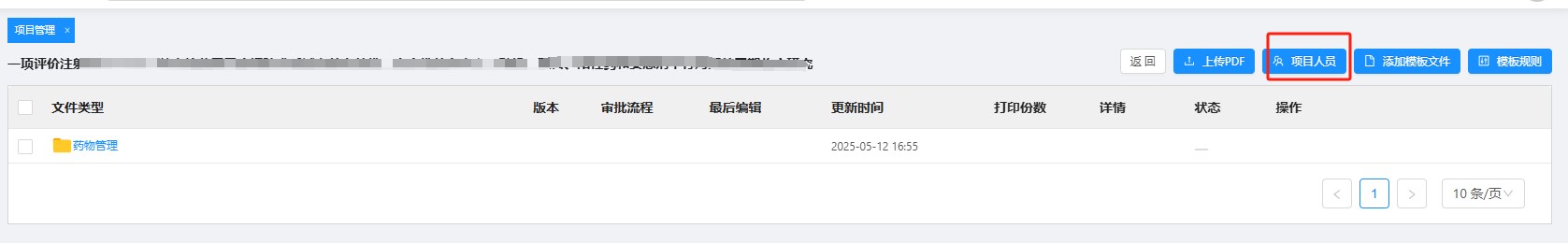
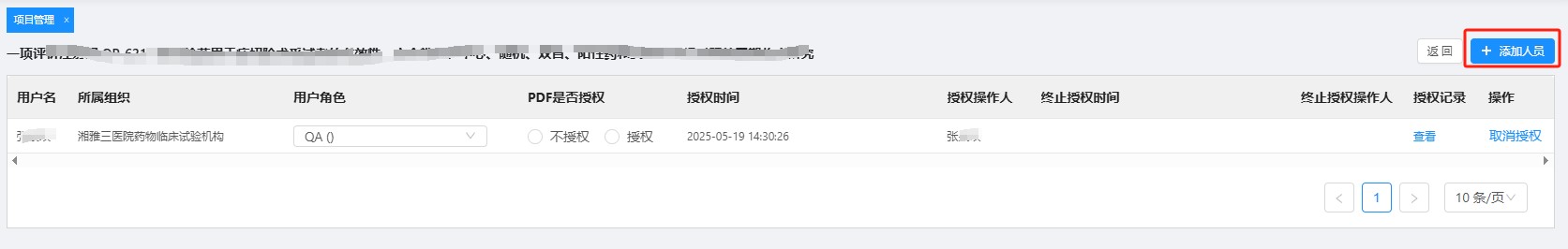
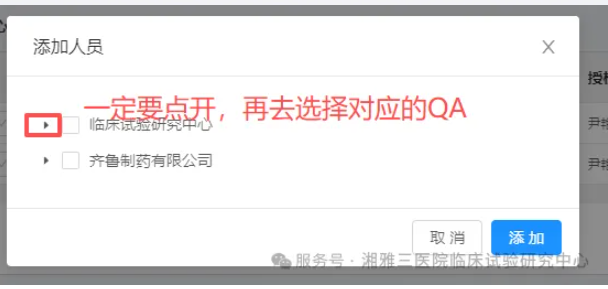
3. 项目创建完成后,创建人须在系统中先点击菜单【项目人员】,页面跳转后,通过【添加人员】关联对应的QA人员(注意:一定点开小三角去选择其中的一个质控员,请勿全选!!),确保项目文件的质量控制流程。
4. 研究团队成员上传命名规范的PDF版受控文档(命名示例:【项目简称】-【项目流水号】-【文件类型(必须和文件里的命名保持一致!!)】-【版本号】-【版本日期】)至项目内。(请注意每个文件单独上传!上传后的文件是不可以删除修改的)
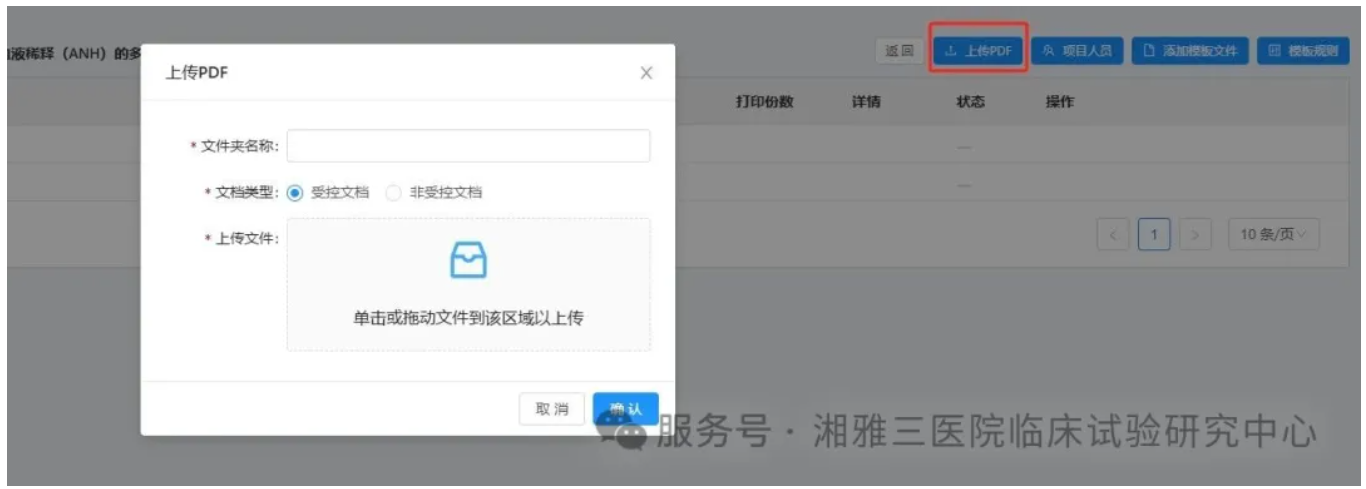
5. 由项目QA人员负责文档的审核及打印(必须由QA进行打印,请勿自行打印!),并填写《临床试验受控文档交接表》。(文档交接表中的文档名称必须和实际上传文件保持一致!!)
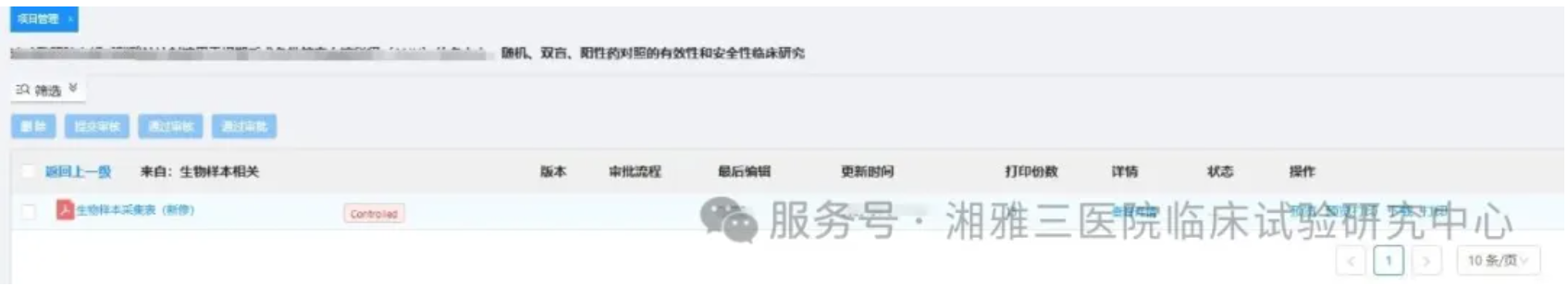
6. 如文档中设计了公司LOGO、版本号、版本日期等,建议在文档页眉体现相关信息,以免遮挡生成的受控编码。(请注意如版本号在页脚左侧需挪至右侧或页眉)
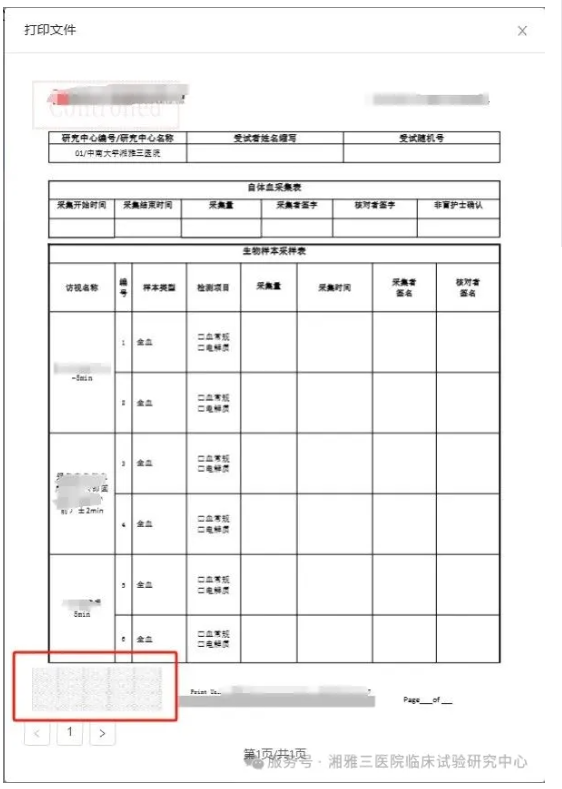
7. 首次打印文档数量按照合同签署的受试者例数或签署例数的50%计算,后续根据实际情况进行打印。打印时,务必选择正确的【目标打印机】。未使用完或损坏的文档须存放至研究者文件夹,无需销毁或回收。
8. 如遇文档管理系统显示已打印但实际未输出文档或文档损坏、丢失等的情况,研究团队成员需在24 h内发送邮件至主要研究者、QA人员(xy3gcpqa@163.com)。邮件名称需包含【专业名称】、【项目简称】及【项目流水号】,正文说明未打印文档的编号、打印和缺失份数、打印人、发生时间等信息。如出现文档遗失情况,参照该流程执行。
9. 文档修订后,研究团队成员需重新上传新版PDF文档(命名规则同前)至项目内,由QA人员负责审核及打印新版本受控文档。
10. 如申办方或CRO公司内部有文档受控管理SOP,参照相关规定执行即可。
![]() 中南大学湘雅三医院临床试验受控文档交接表1.0-2025.6.24.docx
中南大学湘雅三医院临床试验受控文档交接表1.0-2025.6.24.docx